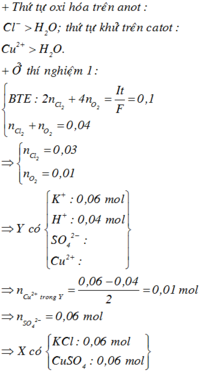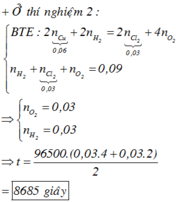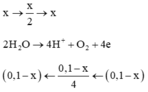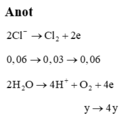Tiến hành điện phân dung dịch chứa a mol KCl và b mol CuSO4 với điện cực trơ, màng ngăn xốp; cường độ dòng điện không đổi I 7,5A, trong thời gian t 4632 giây, thu được dung dịch X; đồng thời ở anot thoát ra 0,12 mol hỗn hợp khí. Nếu thời gian điện phân là 1,5t giây thì tổng số mol khí thoát ra ở hai cực là 0,215 mol. Giả sử trong quá trình điện phân nước bay hơi không đáng kể, hiệu suất điện phân đạt 100%, các khí sinh ra không tan trong nước, bỏ qua sự thủy phân của muối. Cho các phát biểu li...
Đọc tiếp
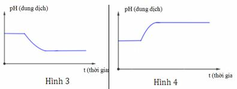
Tiến hành điện phân dung dịch chứa a mol KCl và b mol CuSO4 với điện cực trơ, màng ngăn xốp; cường độ dòng điện không đổi I = 7,5A, trong thời gian t = 4632 giây, thu được dung dịch X; đồng thời ở anot thoát ra 0,12 mol hỗn hợp khí. Nếu thời gian điện phân là 1,5t giây thì tổng số mol khí thoát ra ở hai cực là 0,215 mol. Giả sử trong quá trình điện phân nước bay hơi không đáng kể, hiệu suất điện phân đạt 100%, các khí sinh ra không tan trong nước, bỏ qua sự thủy phân của muối. Cho các phát biểu liên quan đến bài toán:
(a) Tổng khối lượng hai muối trước điện phân là 35,48 gam.
(b) Nếu thời gian điện phân là 1,25t giây thì nước đã điện phân ở cả hai điện cực.
(c) Giá trị của a, b lần lượt là 0,12 và 0,25.
(d) Dung dịch X chỉ có hai chất tan.
(e) Đến thời điểm 1,5t giây, số mol H+ sinh ra ở anot là 0,32 mol.
Số phát biểu sai là
A. 2
B. 4
C. 3
D. 1